医療機器を製造販売する
更新日:2024年9月5日
◆もくじ◆
医療機器を国内で製造販売するには
医療機器を国内で製造して、市場に出荷するには、製造販売業許可と製造業登録の両方が必要となります。
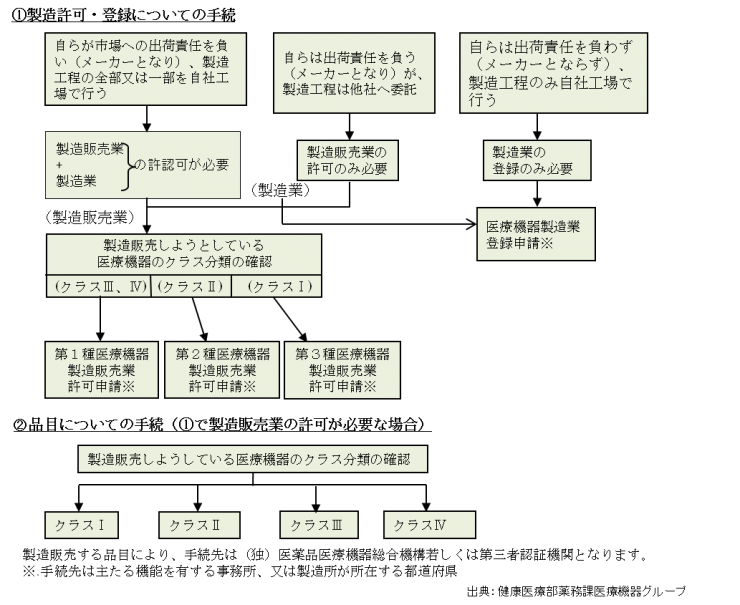
下のフローチャート①製造許可・登録について手続は、行う業務に応じてどの許可や登録が必要になるかを記載したもので、②は医療機器のクラス分類に応じた品目ごとの手続きについて記載したものです。
医療機器製造販売業とは
医療機器を製造(他に委託して製造する場合を含みます)し、または海外で製造された医療機器を輸入した後に、販売業者等に対し医療機器を販売・貸与・授与を行うなどして、医療機器を市場に流通させる役割を担います。プログラム医療機器を電気通信回線を通じて提供する場合も該当します。
製造または輸入した医療機器は、販売業者・貸与業者にのみ販売、貸与、授与でき、医院や一般消費者への販売などはこの許可ではできません。
製造販売業の許可の種類
| クラス | 分類 | 許可の種類 | 申請先 |
| Ⅳ | 高度管理医療機器 | 第一種医療機器製造販売業許可 | 都道府県 |
| Ⅲ | |||
| Ⅱ | 管理医療機器 | 第二種医療機器製造販売業許可 | |
| Ⅰ | 一般医療機器 | 第三種医療機器製造販売業許可 |
製造販売業の許可要件
製造販売業の許可要件については「製造販売業の許可要件」のページを確認ください。
医療機器製造業とは
医療機器製造販売業者から委託を受けて、医療機器を業として製造する製造所は、この医療機器製造業の登録を受ける必要があります。
この医療機器製造業の登録は、企業ごとに受けるのではなく、製造所ごとに受ける必要があります。
対象となる製造工程は、設計・主たる組立・滅菌・最終製品の保管の各工程となっていて、この工程を行う製造所は必ず医療機器製造業登録を受ける必要があります。
平成26年の改正前は、設計工程が含まれていませんでしたが、改正後新たに追加されました。また、改正後は、ラベリングなどの包装・表示工程が対象から外れました。
主たる組立ではない組立工程や部品を製造する製造所については、この製造業登録は必要ありません。
登録対象となる製造所の範囲
製造業が必要となる工程は、設計・主たる組立て・滅菌・最終製品の保管が対象ですが、その定義は以下のようになっています。
| 工程 | 内容 |
| 設計 | 承認又は認証を要する医療機器の設計開発に関して責任を有する者がいる施設であって、当該設計開発に係る記録を管理している場所 |
| 主たる組立て | 製造実態がある施設のうち、当該品目に係る品質管理監督システム又は製品実現について実質的に責任を有する施設 |
| 滅菌 | 滅菌医療機器について、滅菌を行う施設 |
| 最終製品の保管 | 最終製品を保管する施設のうち、市場への出荷判定時に製品を保管している施設 |
製造業の登録の有無は以下のようになります。医療機器の種類によって、どの工程で製造業登録が必要かが変わってきます。
| 製造工程 | 医療機器(右以外) | クラスⅠ医療機器 | 単体プログラム | 単体プログラムの記録媒体 |
| 設計 | 必要 | 不要 | 必要 | 必要 |
| 主たる組立て | 必要 | 必要 | 不要 | 不要 |
| 滅菌 | 必要 | 必要 | 不要 | 不要 |
| 最終製品の保管 | 必要 | 必要 | 不要 | 必要 |
医療機器製造業登録の要件
製造業の登録要件については「製造業の登録要件」のページを確認ください。
医療機器の品目手続き
個々の医療機器を市場へ流通させるためには、上記の許可・登録を受けたうえで、医療機器ごとに手続を行わなければなりません。医療機器は、クラス分類がされており、それに応じた手続きが必要になります。
| クラス | 申請名 | 申請先 |
| 一般医療機器(クラスⅠ) | 製造販売届出 | 医薬品医療機器総合機構(PMDA) |
| 管理医療機器(クラスⅡ) | 製造販売認証申請 | 第三者認証機関 or 医薬品医療機器総合機構(PMDA) |
| 高度管理医療機器(クラスⅢ・Ⅳ) | 製造販売承認申請 | 第三者認証機関 or 医薬品医療機器総合機構(PMDA) |
医療機器に関する許認可のご相談はサポート行政書士法人へ
サポート行政書士法人では、新規で医療機器業界へ参入される方から、既存の製造販売業者・製造業者・販売業者の皆さまに対して、医薬品医療機器等法に関する申請サポートやコンサルティングを行っています。
医療機器の申請は専門性が高く、対応している行政書士が少ない分野の一つと言えます。
日々企業の皆様の代理人として行政庁への申請や折衝を行っている行政書士だからこそ蓄積できるノウハウ・実績を元に、医療機器に関する法務サービスを提供いたします。
弊社の担当者は、全国の都道府県で申請実績があります。ぜひご相談ください。

専任スタッフが全国の案件を対応しています。