医薬品医療機器等法の概要
更新日:2024年9月6日
薬事法から医薬品医療機器等法への改正により、医薬品、医療機器等の安全かつ迅速な提供の確保を図るため、添付文書の届出義務の創設、医療機器の登録認証機関による認証範囲の拡大等の安全対策の強化、医療機器及び体外診断用医薬品の特性を踏まえた規制の構築等が行われました。
◆もくじ◆
医療機器に関する主な改正点
医療機器製造業に関する変更
(1)製造業が、可制・認定制から登録制に変更
これまで、国内製造業は許可制、外国製造業者は認定でしたが、どちらも登録制に改められ、要件が簡素化されました。これまでの様な製造区分は無くなり、製造業の登録すべき範囲(対象)が変更されました。
| 改正前 | 改正後 | |
| 許可・登録等 | 国内:許可、外国:認定 | 国内・外国:登録 |
| 有効期間 | 5年 | 5年 |
| 許可・登録等権者 | 国内:都道府県、外国:国 | 国内:都道府県、外国:国 |
| 製造区分 | 一般、滅菌、生物、包装等 | なし |
| 許可・登録等の要件 | 欠格要件 | 欠格要件 |
| 構造設備要件 (一般・滅菌・生物・包装等の区分ごと) | なし(必要事項は新QMS省令で規定) | |
| 責任技術者 | 必要 | 必要 |
一般、包装等の区分がなくなり、薬事法における許可要件であった薬局等構造設備規則の適用を受けなくなりました。
(2)登録が必要な製造工程の変更
これまで許可等の対象ではなかった「設計」を行う施設も登録対象になり、「プログラム」及び「プログラムを記録した記録媒体」についても医療機器として登録が必要になりました。
| 製造工程 | ①医療機器 (②③④以外) | ②一般医療機器 | ③単体プログラム | ④単体プログラムの記録媒体 |
| 設計 | ○ | × | ○ | ○ |
| 主たる組立て | ○ | ○ | × | × |
| 滅菌 | ○ | ○ | × | × |
| 国内における最終製品の保管 | ○ | ○ | × | ○ |
医療機器の定義に関する変更
薬事法では規制対象外となっていた「プログラム」そのものについて、国際整合性も踏まえ法律の規制対象とし、医療機器の定義に「プログラム」及び「これを記録した記録媒体」が追加されました。
医療機器に該当するプログラムの範囲は以下の通りです。
プログラム
1.疾病診断用プログラム
2.疾病治療用プログラム
3.疾病予防用プログラム
プログラムを記録した記録媒体
1.疾病診断用プログラムを記録した記録媒体
2.疾病治療用プログラムを記録した記録媒体
3.疾病予防用プログラムを記録した記録媒体
医療機器製造販売業に係る許可要件・遵守事項の見直し等(QMS関係等)
QMS制度の再編
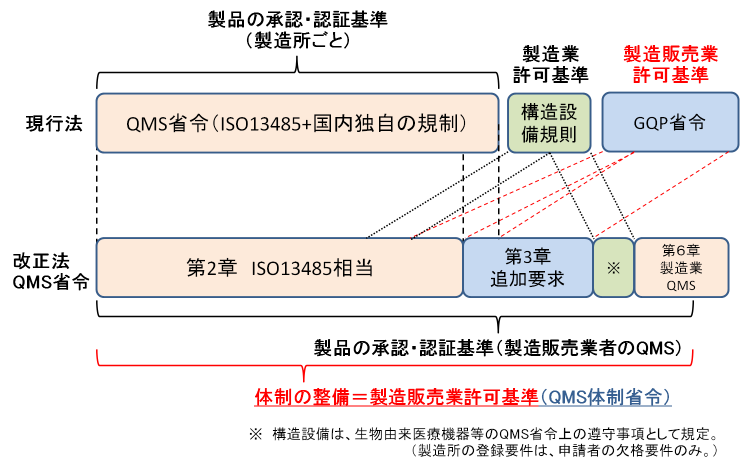
医療機器の製造管理及び品質管理の基準への適合性調査は、これまでの「製造所ごとの調査」に代わって、製品に係る製造販売業者及びすべての登録製造所を含む品質管理監督システムごとに調査を行う新たな規制体系が適用されることとなりました。
(1)QMS省令が改正され、製造販売業に対して適用されることとなりました。
これまで医療機器製造販売業者には、GQP・GVP手順書に基づく記録が求めらていましたが、GQPがQMSに変更となり、関連する製造業者を一体とした品質管理監督システム基準書(品質マニュアル)の構築が必要となっています。
(2)医療機器等の製造販売業の許可要件として、GQP省令に代わり、QMS体制省令に適合していることが加わりました。
医療機器又は体外診断用医薬品の製造管理又は品質管理に係る業務を行う体制の基準に関する省令(平成26年8月8日厚生労働省令第94号) は一般医療機器のみを取り扱う製造販売業者、製造業者についても適用されます。
(3)製品群による調査の合理化
製品群省令(医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律第23条の2の5第7項第1号に規定する医療機器又は体外診断用医薬品の区分を定める省令)が制定され、同一製品群・同一登録製造所の製品については、調査が不要になりました。
医療機器の認証制度に関する変更
(1)登録認証機関による第三者認証の対象が拡大されました。
管理医療機器だけでなく、「厚生労働大臣が基準を定めて指定する高度管理医療機器」まで、民間の登録認証機関による認証の対象になりました。
(2)薬事法においては承認品目については取得者の地位の承継が認められていましたが、医薬品医療機器等法では認証品目についても承継が可能となります。
医療機器の販売・貸与業に対する規制
対価を得る賃貸だけでなく、反復継続的に対価を得ずに貸与を行う場合も、許可又は届出の対象となり、名称も、賃貸業から貸与業に変更されました。
医療機器に関する許認可のご相談はサポート行政書士法人へ
サポート行政書士法人では、新規で医療機器業界へ参入される方から、既存の製造販売業者・製造業者・販売業者の皆さまに対して、医薬品医療機器等法に関する申請サポートやコンサルティングを行っています。
医療機器の申請は専門性が高く、対応している行政書士が少ない分野の一つと言えます。
日々企業の皆様の代理人として行政庁への申請や折衝を行っている行政書士だからこそ蓄積できるノウハウ・実績を元に、医療機器に関する法務サービスを提供いたします。
弊社の担当者は、全国の都道府県で申請実績があります。ぜひご相談ください。

専任スタッフが全国の案件を対応しています。