许认可的各责任者
更新日:2024年3月20日
◆もくじ◆
总制造贩卖责任人/日本品质业务运营责任人/管理监督人/管理责任人的兼任
以下情况下,可以兼任总制造贩卖责任人/日本品质业务运营责任人/管理监督人/管理责任人。
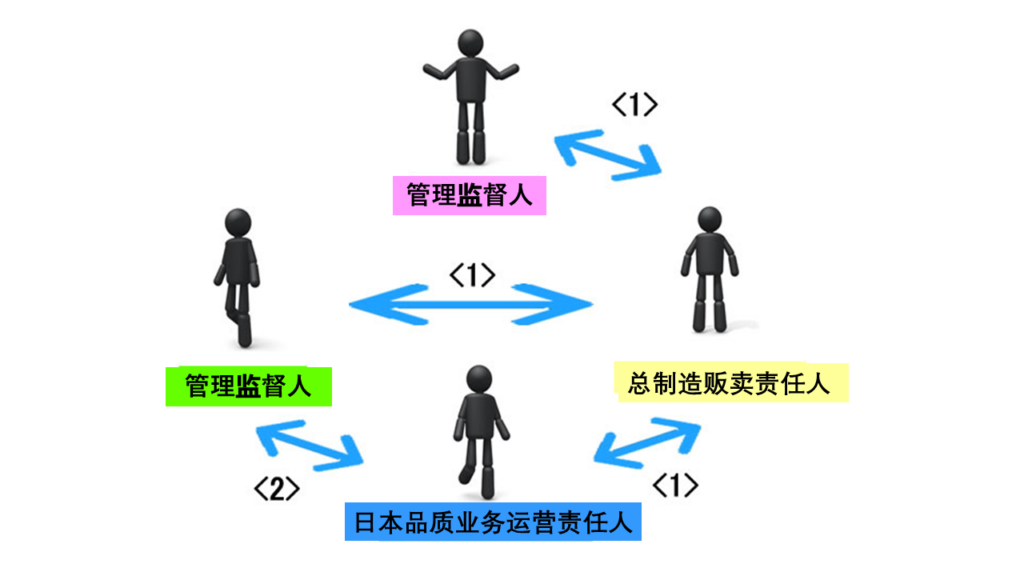
| <1> | 总制造贩卖责任人可以同时兼任管理监督人或管理责任人或日本品质业务运营责任人。 |
| <2> | 日本品质业务运营责任人可以同时兼任管理责任人。 |
| <3> | 总制造贩卖责任人可以同时兼任管理监督人、管理责任人及日本品质业务运营责任人中的2或3个以上职位,只要这不影响各自的职责。 |
总制造贩卖责任人/日本品质业务运营责任人/安全管理责任人/责任技术人的兼任
以下情况下,可以兼任总制造贩卖责任人/日本品质业务运营责任人/安全管理责任人/责任技术人。
| 第一种医疗器械制造贩卖业者 | 可以同时兼任总制造贩卖责任人和日本品质业务运营责任人 |
| 第二种医疗器械制造贩卖业者 | 可以同时兼任总制造贩卖责任人和日本品质业务运营责任人,只要不兼任日本品质业务运营责任人时,则可以同时兼任总制造贩卖责任人和安全管理责任人。 |
| 第三种医疗器械制造贩卖业者 | 可以同时兼任总制造贩卖责任人、日本品质业务运营责任人及安全管理责任人 |
| 国内品质业务运营责任人和责任技术人 | 如果制造所与开展业务的事务所在同一设施内,则可以同时兼任日本品质业务运营责任人和责任技术人 |
总制造贩卖责任人的要件
| 医疗器械制造贩卖业 | 资格要件 | |
| 第一种 第二种 | ① | 在大学或高等专门学校完成物理学、化学、生物学、工程学、信息学、冶金学、电气工程、机械学、药学、医学或牙医学的专业课程。 |
| ② | 在高中完成物理、化学、生物、工程、信息学、冶金、电气工程、机械、药学、医学或牙科的专业课程,并在医药品或医疗器械的质量管理或上市后安全管理方面工作了工作了3年以上。 | |
| ③ | 从事与医药产品或医疗器械的质量控管理或上市后安全管理有关的工作5年以上,并且完成了由厚生劳动大臣注册的人员举办的培训课程。 | |
| ④ | 厚生劳动大臣认可的人。 | |
| 第三种 | ① | 在高中完成物理、化学、生物、工程、信息学、冶金、电气工程、机械、药学、医学或牙科的专业课程。 |
| ② | 在高中完成物理、化学、生物、工程、信息学、冶金、电气工程、机械、药学、医学或牙科等相关科目,且从事医药品,医药部外品、化妆品或医疗器械的质量管理或上市后安全管理有关的工作3年以上。 | |
| ③ | 厚生劳动大臣认可的人。 | |
日本品质业务运营责任人的要件
日本品质业务运营责任人负责医疗器械的品质管理业务,以及做出将设备投放市场和召回处理等决定。
由于品质管理业务需要知识和经验,因此需要指派一个有工作经验的人。
日本品质业务运营责任人需要满足以下条件。
| ① | 是在制造贩卖业者的品质保证部门的负责人 |
| ② | 从事品质管理业务或其他类似业务3年以上 |
| ③ | 有确保日本的品质管理业务正常顺利开展的能力 |
| ④ | 非医疗器械等销售相关部门的成员,也不存在其他可能妨碍日本的品质管理业务正常顺利开展的情形。 |
QMS施行通知就 “②从事品质管理业务或其他类似业务3年以上”做出了如下规定。
以下责任人或从事该业务的人符合“从事品质管理业务或其他类似业务3年以上”规定。
另外,“3年以上”是指在从事相关业务的累计年限,不论实在本公司还是其他公司。
a. 管理监督人
b. 管理责任人
c. 医疗器械等的总制造贩卖责任人
d. 旧法所规定的品质保证责任人、制造管理者及责任技术人。
e. 从事与制造商或经销商的制造管理或品质管理有关的工作的其他人员。
f. 在已通过ISO 9001或ISO 13485认证的企业经营者等处(仅限于从事产品制造、销售或生产的企业,不包括仅从事提供服务的企业等)从事有关品质管理系统的持续改进或维护工作的人员。
安全管理责任人的要件
制造与销售高度管理医疗器械(III、IV类)的安全管理责任人的资格要件
满足以下①到④的所有条件的人才有资格任职。
| ① | 是总体安全管理部门的责任人 |
| ② | 从事安全保障业务或其他类似业务3年以上 |
| ③ | 有确保安全保障业务正常顺利开展的能力 |
| ④ | 非医疗器械的销售相关部门的成员,也不存在其他可能妨碍日本的安全保障业务正常顺利开展的情形。 |
制造销售管理医疗器械(II类)、一般医疗器械(I类)的安全管理责任人的资格要件
满足以下①②的所有条件的人才有资格任职。
| ① | 有确保安全保障业务正常顺利开展的能力 |
| ② | 非医疗器械的销售相关部门的成员,也不存在其他可能妨碍日本的安全保障业务正常顺利开展的情形。 |
咨询有关医疗器械的许可、认可及承认等相关事宜,请联系我们。
我们向新进入医疗器械行业的企业,以及现有的制造商、生产商和经销商提供与医药品医疗器械等法相关的申请支持和咨询服务。
医疗器械的申请具有高度专业性,能够完美处理这些业务的行政书士较少。
而我们提供医疗器械相关的法律服务的基础是我们作为企业代理人向日本行政机关申请与斡旋沟通时所积累的丰富经验和优秀业绩。
我们的团队拥有在全国各都道府县的申请经验。请务必与我们联系以获取更多信息。

专任人员处理全日本的案件